При входе на сайт вы даете согласие на обработку персональных данных в соответствии с пользовательским соглашением
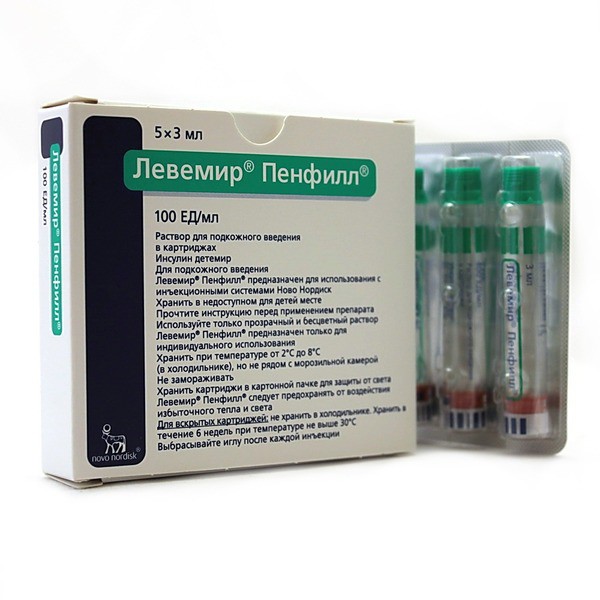
Внешний вид упаковки может отличаться от фотографии
Левемир® Пенфилл® |
Novo Nordisk (Дания)
раствор для подкожного введения 100 ЕД/мл; картридж 3 мл, блистер 5, пачка картонная 1; код EAN: 4602206000943; № ЛС-000597, 2010-01-18 от Novo Nordisk (Дания)
Латинское название
Действующее вещество
АТХ:
Фармакологическая группа
Нозологическая классификация (МКБ-10)
E11 Инсулинонезависимый сахарный диабет
Состав
| Раствор для подкожного введения | 1 мл |
| активное вещество: | |
| инсулин детемир | 100 ЕД (14,2 мг) |
| (1 картридж содержит 3 мл раствора, эквивалентного 300 ЕД) | |
| (1 ЕД содержит 0,142 мг бессолевого инсулина детемир, что соответствует одной единице человеческого инсулина (МЕ). | |
| вспомогательные вещества: глицерол — 16 мг; фенол — 1,8 мг; метакрезол — 2,06 мг; цинка ацетат — 65,4 мкг; натрия гидрофосфата дигидрат — 0,89 мг; натрия хлорид — 1,17 мг; кислота хлористоводородная или натрия гидроксид — q.s.; вода для инъекций — до 1 мл |
Описание лекарственной формы
Прозрачный, бесцветный раствор.
Фармакологическое действие
Фармакодинамика
Препарат Левемир® Пенфилл® производится методом биотехнологии рекомбинантной ДНК с использованием штамма Saccharomyces cerevisiae. Является растворимым базальным аналогом человеческого инсулина пролонгированного действия с плоским профилем действия. Профиль действия препарата Левемир® Пенфилл® значительно менее вариабелен по сравнению с изофан-инсулином и инсулином гларгин.
Пролонгированное действие препарата Левемир® Пенфилл® обусловлено выраженной самоассоциацией молекул инсулина детемир в месте инъекции и связыванием молекул препарата с альбумином посредством соединения с боковой жирнокислотной цепью. Инсулин детемир по сравнению с изофан-инсулином к периферическим тканям-мишеням поступает медленнее. Эти комбинированные механизмы замедленного распределения обеспечивают более воспроизводимый профиль абсорбции и действия препарата Левемир® Пенфилл® по сравнению с изофан-инсулином.
Для доз 0,2–0,4 ЕД/кг 50% от максимального эффекта препарата наступает в интервале от 3–4 до 14 ч после введения. Продолжительность действия составляет до 24 ч, в зависимости от дозы, что обеспечивает возможность однократного и двукратного ежедневного введения. При двукратном введении Css препарата достигается после введения 2–3 доз препарата.
После п/к введения наблюдался фармакодинамический ответ, пропорциональный введенной дозе (максимальный эффект, продолжительность действия, общий эффект).
В длительных исследованиях были продемонстрированы низкие показатели вариабельности концентрации глюкозы плазмы натощак день ото дня при лечении пациентов препаратом Левемир® Пенфилл® в отличие от изофан-инсулина.
В длительных исследованиях у пациентов с сахарным диабетом типа 2, получавших терапию базальным инсулином в комбинации с пероральными гипогликемическими препаратами, было продемонстрировано, что гликемический контроль (по показателю гликозилированного гемоглобина — НbА1с) на фоне терапии препаратом Левемир® Пенфилл® был сравним с таковым при лечении изофан-инсулином и инсулином гларгин с низким приростом массы тела (см. табл. 1).
Таблица 1
Изменение массы тела при инсулинотерапии
| Длительность исследования, нед | Изменение массы тела, кг | |||
| Инсулин детемир 1 раз в сутки | Инсулин детемир 2 раза в сутки | Инсулин-изофан | Инсулин гларгин | |
| 20 | +0,7 | +1,6 | ||
| 26 | +1,2 | +2,8 | ||
| 52 | +2,3 | +3,7 | +4 | |
В исследованиях применение комбинированной терапии препаратом Левемир® Пенфилл® и пероральными гипогликемическими препаратами привело к снижению риска развития легкой ночной гипогликемии на 61–65% в сравнении с применением изофан-инсулина.
Было проведено открытое рандомизированное клиническое исследование с участием пациентов с сахарным диабетом типа 2, не достигших целевых показателей гликемии на фоне терапии пероральными гипогликемическими препаратами. Исследование началось с 12-недельного подготовительного периода, во время которого пациенты получали комбинированную терапию лираглутидом в сочетании с метформином, и на фоне которой 61% пациентов достиг показателя НbА1с <7%. 39% пациентов, не достигших целевых значений гликемии на фоне проведенной комбинированной терапии лираглутидом с метформином, были рандомизированы в 2 терапевтические группы для получения дальнейшего лечения. Пациентам одной из терапевтических групп дополнительно к терапии лираглутидом с метформином был назначен препарат Левемир® Пенфилл® в ежедневной однократной дозе; пациенты другой продолжали получать лираглутид в комбинации с метформином в течение последующих 52 нед. На протяжении этого периода терапевтическая группа, получавшая дополнительно к терапии лираглутидом с метформином ежедневную однократную инъекцию препарата Левемир® Пенфилл®, продемонстрировала дальнейшее снижение показателя НbА1с с исходных 7,6% до уровня 7,1% в конце 52-недельного периода, при отсутствии эпизодов тяжелой гипогликемии. При добавлении дозы препарата Левемир® Пенфилл® к терапии лираглутидом сохранялось преимущество последнего в отношении статистически значимого уменьшения массы тела у пациентов (см. табл. 2).
Таблица 2
Данные клинических исследований — терапия препаратом Левемир® Пенфилл®, назначенная дополнительно к комбинированной схеме лечения лираглутидом с метформином
| Показатели | Недели лечения | Пациенты, рандомизированне для получения терапии препаратом Левемир® Пенфилл® в дополнение к терапии лираглутид+метформин, N=160 | Пациенты, рандомизированне для получения терапии лираглутид+метформин, N=149 | Коэффициент достоверности изменений (p-value) |
| Среднее изменение значения показателя HbA1c по сравнению с исходной точкой испытания, % | 0–26 | -0,51 | +0,02 | <0,0001 |
| 0–52 | -0,5 | 0,01 | <0,0001 | |
| Соотношение пациентов, достигших целевого значения показателя HbA1c <7%, % | 0–26 | 43,1 | 16,8 | <0,0001 |
| 0–52 | 51,9 | 21,5 | <0,0001 | |
| Изменение массы тела пациентов по сравнению с показателями в исходной точке испытания, кг | 0–26 | -0,16 | -0,95 | 0,0283 |
| 0–52 | -0,05 | -1,02 | 0,0416 | |
| Эпизоды легкой гипогликемии (на количество пациенто-лет экспозиции испытуемого препарата) | 0–26 | 0,286 | 0,029 | 0,0037 |
| 0–52 | 0,228 | 0,034 | 0,0011 |
В долгосрочных исследованиях (>6 мес) с участием пациентов с сахарным диабетом типа 1 показатель концентрации глюкозы в плазме крови натощак был лучше на фоне лечения препаратом Левемир® Пенфилл® по сравнению с применением изофан-инсулина в базис-болюсной терапии. Гликемический контроль (НbА1с) на фоне терапии препаратом Левемир® Пенфилл® был сравним с таковым при лечении изофан-инсулином, но с более низким риском развития ночной гипогликемии и отсутствием увеличения массы тела на фоне применения препарата Левемир® Пенфилл®.
Результаты клинических исследований по оценке базис-болюсного режима инсулинотерапии свидетельствуют о сопоставимой частоте развития гипогликемий в целом на фоне терапии препаратом Левемир® Пенфилл® и изофан-инсулином. Анализ развития ночных гипогликемий у пациентов с сахарным диабетом типа 1 продемонстрировал значительно более низкую частоту развития легких ночных гипогликемий на фоне применения препарата Левемир® Пенфилл® (когда пациент самостоятельно может устранить состояние гипогликемии и гипогликемия подтверждена результатом измерения концентрации глюкозы в капиллярной крови — менее 2,8 ммоль/л или глюкозы в плазме крови — менее 3,1 ммоль/л), по сравнению с таковой при применении изофан-инсулина; при этом между двумя исследуемыми препаратами не выявлено различий по частоте наступления эпизодов легких ночных гипогликемий у пациентов с сахарным диабетом типа 2. Профиль ночной гликемии является более плоским и ровным у препарата Левемир® Пенфилл® по сравнению с изофан-инсулином, что отражается в более низком риске развития ночной гипогликемии. При применении препарата Левемир® Пенфилл® наблюдалась выработка антител. Однако этот факт никак не влияет на гликемический контроль.
Беременность
В ходе рандомизированного контролируемого клинического исследования, включающего 310 беременных женщин с сахарным диабетом типа 1, проводилась оценка эффективности и безопасности препарата Левемир® Пенфилл® в базис-болюсном режиме терапии (152 пациентки), по сравнению с изофан-инсулином, в комбинации с инсулином аспарт (158 пациенток), применяемым в качестве прандиального инсулина.
Результаты исследования показали, что у пациенток, получавших препарат Левемир® Пенфилл®, отмечено схожее по сравнению с группой, получающей изофан-инсулин, снижение показателя НbА1с на 36-й нед беременности. Группа пациенток, получавших терапию препаратом Левемир® Пенфилл®, и группа, получавшая терапию изофан-инсулином, на протяжении всего периода беременности демонстрировали сходство по общему профилю НbА1с.
Целевой уровень НbА1с <6% на 24-й и 36-й нед беременности был достигнут у 41% пациенток в группе терапии препаратом Левемир® Пенфилл® и у 32% пациенток в группе терапии изофан-инсулином.
Концентрация глюкозы натощак на сроках беременности 24 и 36 нед был статистически значимо ниже в той группе женщин, которая принимала препарат Левемир® Пенфилл®, по сравнению с группой, получавшей терапию изофан-инсулином. В течение всего периода беременности не было выявлено статистически значимых различий между пациентками, получавшими препарат Левемир® Пенфилл® и изофан-инсулин, по частоте развития эпизодов гипогликемий.
Обе группы беременных женщин, получавшие лечение препаратом Левемир® Пенфилл® и изофан-инсулином, продемонстрировали аналогичные результаты по частоте наступления у них нежелательных явлений в течение всего периода беременности; однако выявлено, что в количественном отношении частота наступления серьезных нежелательных явлений у пациенток в течение всего срока беременности (61 (40%) против 49 (31%), у детей в течение периода внутриутробного развития и после рождения (36 (24%) против 32 (20%) была выше в группе лечения препаратом Левемир® Пенфилл® по сравнению с группой терапии изофан-инсулином.
Количество живорожденных детей от матерей, которые забеременели уже после того, как были рандомизированы в терапевтические группы для получения лечения одним из испытуемых препаратов, составило 50 (83%) в группе лечения препаратом Левемир® Пенфилл® и 55 (89%) — в группе лечения изофан-инсулином. Количество детей, родившихся с врожденными пороками развития, составило 4 (5%) в группе лечения препаратом Левемир® Пенфилл® и 3 (2%) — в группе лечения изофан-инсулином.
Дети и подростки
Эффективность и безопасность применения препарата Левемир® Пенфилл® у детей была изучена в ходе 2 контролируемых клинических исследований продолжительностью 12 мес с участием подростков и детей в возрасте старше двух лет, страдающих сахарным диабетом типа 1 (всего 694 пациента); одно из этих исследований включало в общей сложности 82 ребенка с сахарным диабетом типа 1 в возрастной категории от 2 до 5 лет. Результаты этих исследований продемонстрировали, что гликемический контроль (HbA1c) на фоне терапии препаратом Левемир® Пенфилл® был сравним с таковым при лечении изофан-инсулином при их назначении в базис-болюсной терапии. Кроме того, отмечен более низкий риск развития ночной гипогликемии (на основании значений концентрации глюкозы в плазме, измеренных пациентами самостоятельно) и отсутствие прироста массы тела (стандартное отклонение для массы тела, скорректированной в соответствии с полом и возрастом пациента) на фоне лечения препаратом Левемир® Пенфилл® по сравнению с применением изофан-инсулина. Одно из клинических исследований было продлено еще на 12 мес (в общей сложности получены клинические данные за 24 мес) с целью получения более полной базы данных для проведения оценки образования у пациентов антител на фоне долговременного лечения препаратом Левемир® Пенфилл®.
Полученные в ходе исследования результаты свидетельствуют о том, что в течение первого года лечения на фоне приема препарата Левемир® Пенфилл® произошло увеличение уровня антител к инсулину детемир; однако к концу 2-го года лечения уровень образования антител к препарату Левемир® Пенфилл® снизился у пациентов до уровня, незначительно превышающего исходный на момент начала терапии препаратом Левемир® Пенфилл®. Таким образом, доказано, что образование антител у больных сахарным диабетом на фоне лечения препаратом Левемир® Пенфилл® не оказывает отрицательного влияния на уровень гликемического контроля и дозу инсулина детемир.
Фармакокинетика
Абсорбция
Cmax в плазме крови достигается через 6–8 ч после введения.
При двукратном ежедневном режиме введения Css препарата в плазме крови достигается после 2–3 введений.
Внутрииндивидуальная вариабельность всасывания ниже у препарата Левемир® Пенфилл® по сравнению с другими препаратами базального инсулина.
Клинически значимых межполовых различий в фармакокинетике препарата Левемир® Пенфилл® выявлено не было.
Распределение
Средний Vd препарата Левемир® Пенфилл® (приблизительно 0,1 л/кг) указывает на то, что высокая доля инсулина детемир циркулирует в крови.
Метаболизм
Инактивация препарата Левемир® Пенфилл® сходна с таковой у препаратов человеческого инсулина; все образующиеся метаболиты являются неактивными.
Результаты исследований связывания белков in vitro и in vivo показывают отсутствие клинически значимых взаимодействий между инсулином детемир и жирными кислотами или другими препаратами, связывающимися с белками.
Выведение
Терминальный T1/2 после п/к инъекции определяется степенью всасывания из подкожной ткани и составляет 5–7 ч в зависимости от дозы.
Линейность
При п/к введении концентрации в плазме крови были пропорциональны введенной дозе (Cmax, степень всасывания).
Не выявлено фармакокинетическое или фармакодинамическое взаимодействие между лираглутидом и препаратом Левемир® Пенфилл®, в равновесном состоянии, при одновременном введении пациентам с сахарным диабетом типа 2 препарата Левемир® Пенфилл® в однократной дозе 0,5 ЕД /кг и лираглутида в дозе 1,8 мг.
Особые группы пациентов
Фармакокинетические свойства препарата Левемир® Пенфилл® были исследованы у детей (6–12 лет) и подростков (13–17 лет) и сравнены с фармакокинетическими свойствами у взрослых с сахарным диабетом типа 1. Различий не выявлено.
Клинически значимых различий в фармакокинетике препарата Левемир® Пенфилл® между пожилыми и молодыми пациентами или между пациентами с нарушениями функции почек и печени и здоровыми пациентами не выявлено.
Данные доклинических исследований по безопасности
Исследования in vitro, в человеческой клеточной линии, включая исследования по связыванию с рецепторами инсулина и ИФР-1 (инсулиноподобный фактор роста), показали, что инсулин детемир имеет низкое сродство к обоим рецепторам и мало влияет на рост клеток по сравнению с человеческим инсулином. Доклинические данные, основанные на обычных исследованиях фармакологической безопасности, токсичности повторных доз, генотоксичности, канцерогенного потенциала, токсического влияния на репродуктивную функцию, не выявили какой-либо опасности для человека.
Показания препарата Левемир® Пенфилл®
Сахарный диабет у взрослых, подростков и детей старше 2 лет.
Противопоказания
повышенная индивидуальная чувствительность к инсулину детемир или любому из компонентов препарата;
детский возраст до 2 лет (клинические исследования у данной группы пациентов не проводились).
Применение при беременности и кормлении грудью
При применении препарата Левемир® Пенфилл® во время беременности необходимо учитывать, насколько преимущества его применения перевешивают возможный риск.
Одно из рандомизированных контролируемых клинических исследований с участием беременных женщин с сахарным диабетом типа 1, в ходе которого изучались эффективность и безопасность комбинированной терапии препаратом Левемир® Пенфилл® с инсулином аспарт (152 беременных) по сравнению с терапией изофан-инсулином в сочетании с инсулином аспарт (158 беременных), не выявило различий в общем профиле безопасности во время беременности, в исходах беременности или влиянии на здоровье плода и новорожденного (см. «Фармакодинамика», «Фармакокинетика»).
Дополнительные данные по эффективности и безопасности лечения препаратом Левемир® Пенфилл®, полученные приблизительно от 300 беременных женщин в период постмаркетингового применения, свидетельствуют об отсутствии нежелательных побочных эффектов инсулина детемир, приводящих к возникновению врожденных пороков развития и мальформативной или фето/неонатальной токсичности.
Исследования репродуктивной функции у животных не выявили токсического действия препарата на репродуктивную систему (см. «Фармакодинамика», «Фармакокинетика»).
В целом, необходимо тщательное наблюдение беременных женщин с сахарным диабетом в течение всего срока беременности, а также при планировании беременности. Потребность в инсулине в I триместре беременности обычно уменьшается, затем во II и III триместрах возрастает. Вскоре после родов потребность в инсулине быстро возвращается к уровню, который был до беременности.
Неизвестно, выделяется ли инсулин детемир с грудным молоком. Предполагается, что инсулин детемир не влияет на метаболические реакции в организме новорожденных/младенцев в период грудного вскармливания, поскольку он относится к группе пептидов, которые легко расщепляются в пищеварительном тракте на аминокислоты и усваиваются организмом.
У кормящих женщин может потребоваться коррекция дозы инсулина и диеты.
Побочные действия
Побочные реакции, наблюдаемые у пациентов, применяющих препарат Левемир®, в основном развиваются вследствие фармакологического эффекта инсулина. Доля пациентов, получающих лечение и у которых ожидается развитие побочных реакций, оценивается как 12%.
Наиболее частой побочной реакцией, которая развивается во время лечения препаратом Левемир®, является гипогликемия (см. раздел ниже).
Из клинических исследований известно, что тяжелые гипогликемии, требующие вмешательства третьих лиц, развиваются приблизительно у 6% пациентов, получающих Левемир®.
Реакции в местах введения могут наблюдаться чаще при лечении препаратом Левемир®, нежели при введении препаратов человеческого инсулина. Эти реакции включают боль, покраснение, крапивницу, воспаление, кровоподтеки, припухлость и зуд в месте инъекции. Большинство реакций в местах введения незначительны и носят транзиторный характер, т.е. обычно исчезают при продолжении лечения в течение от нескольких дней до нескольких недель.
На начальной стадии инсулинотерапии могут возникать нарушения рефракции и отеки. Эти симптомы обычно носят транзиторный характер. Быстрое улучшение контроля гликемии может приводить к состоянию острой болевой нейропатии, которая обычно является обратимой. Интенсификация инсулинотерапии с резким улучшением контроля углеводного обмена может привести к временному ухудшению состояния диабетической ретинопатии, в то же время длительное улучшение контроля гликемии снижает риск прогрессирования диабетической ретинопатии.
Перечень побочных реакций представлен в таблице.
Все представленные ниже побочные реакции, основанные на данных, полученных в ходе клинических испытаний, распределены по группам согласно частоте развития в соответствии с MedDRA и системами органов. Частота развития побочных реакций определена как: очень часто (≥1/10); часто (≥1/100 до <1/10); нечасто (≥1/1000 до <1/100); редко (≥1/10000 до <1/1000); очень редко (<1/10000) и неизвестно (невозможно оценить на основании имеющихся данных) (см. табл. 4).
Таблица 4
| Со стороны иммунной системы | Нечасто — аллергические реакции, потенциально аллергические реакции, крапивница, кожная сыпь, высыпания на коже* |
| Очень редко — анафилактические реакции* | |
| Со стороны обмена веществ и питания | Очень часто — гипогликемия |
| Со стороны нервной системы | Редко — периферическая нейропатия (острая болевая нейропатия) |
| Со стороны органа зрения | Нечасто — нарушения рефракции |
| Нечасто — диабетическая ретинопатия | |
| Со стороны кожи и подкожных тканей | Нечасто — липодистрофия |
| Общие расстройства и нарушения в месте введения | Часто — реакции в местах введения |
| Нечасто — отеки |
* см. Описание отдельных побочных реакций.
Описание отдельных побочных реакций
Аллергические реакции, потенциально аллергические реакции, крапивница, кожная сыпь, высыпания на коже. При использовании препарата Левемир® в базис-болюсном режиме терапии отмечено нечастое развитие аллергических реакций, потенциально аллергических реакций, крапивницы, кожной сыпи и высыпаний на коже. Однако данные, полученные в ходе 3 клинических испытаний, показали частое наступление побочных реакций при применении препарата Левемир® в составе комбинированной терапии с другими пероральными гипогликемическими препаратами (2,2% аллергических реакций и потенциально аллергических реакций).
Анафилактические реакции. Реакции генерализованной гиперчувствительности (в т.ч. генерализованная кожная сыпь, зуд, потливость, желудочно-кишечные расстройства, ангионевротический отек, затруднения дыхания, учащенное сердцебиение, снижение АД) встречаются очень редко, но являются потенциально опасными для жизни.
Гипогликемия. Гипогликемия является наиболее часто встречающейся побочной реакцией. Она может развиться, если доза инсулина слишком высока по отношению к потребности в инсулине. Тяжелая гипогликемия может приводить к потере сознания и/или судорогам, временному или необратимому нарушению функции головного мозга или даже смерти. Симптомы гипогликемии, как правило, развиваются внезапно. Они включают холодный пот, бледность кожных покровов, повышенную утомляемость, нервозность или тремор, чувство тревоги, необычную усталость или слабость, нарушение ориентации, снижение концентрации внимания, сонливость, выраженное чувство голода, нарушение зрения, головную боль, тошноту, учащенное сердцебиение.
Липодистрофия. Липодистрофия (в т.ч. липогипертрофия, липоатрофия) может развиваться в месте инъекции. Соблюдение правил смены места инъекции в пределах одной области может помочь уменьшить риск развития этой побочной реакции.
Взаимодействие
Имеется ряд ЛС, которые влияют на потребность в инсулине.
Гипогликемическое действие инсулина усиливают пероральные гипогликемические препараты, ингибиторы МАО, ингибиторы АПФ, ингибиторы карбоангидразы, неселективные бета-адреноблокаторы, бромокриптин, сульфонамиды, анаболические стероиды, тетрациклины, клофибрат, кетоконазол, мебендазол, пиридоксин, теофиллин, циклофосфамид, фенфлурамин, препараты лития, салицилаты.
Гипогликемическое действие инсулина ослабляют пероральные контрацептивы, ГКС, йодсодержащие тиреоидные гормоны, соматропин, тиазидные диуретики, гепарин, трициклические антидепрессанты, симпатомиметики, даназол, клонидин, БКК, диазоксид, морфин, фенитоин, никотин.
Октреотид/ланреотид может как повышать, так и снижать потребность организма в инсулине.
Бета-адреноблокаторы могут маскировать симптомы гипогликемии и задерживать восстановление после гипогликемии.
Алкоголь может усиливать и пролонгировать гипогликемический эффект инсулина.
Несовместимость. Некоторые ЛС, например содержащие тиоловую или сульфитную группы, при добавлении к препарату Левемир® Пенфилл® могут вызывать разрушение инсулина детемир. Левемир® Пенфилл® не следует добавлять в инфузионные растворы. Этот препарат нельзя смешивать с другими ЛС.
Способ применения и дозы
П/к.
Доза препарата Левемир® Пенфилл® должна подбираться индивидуально в каждом конкретном случае, на основании потребностей пациента.
На основании результатов исследований, ниже представлены рекомендации по титрованию доз (см. табл. 3).
Таблица 3
| Средние значения глюкозы плазмы, измеренные самостоятельно перед завтраком | Коррекция дозы препарата Левемир® Пенфилл®, ЕД |
| >10,0 ммоль/л (180 мг/дл) | +8 |
| 9,1–10 ммоль/л (163–180 мг/дл) | +6 |
| 8,1–9 ммоль/л (145–162 мг/дл) | +4 |
| 7,1–8 ммоль/л (127–144 мг/дл) | +2 |
| 6,1–7 ммоль/л (109–126 мг/дл) | +2 |
| 4,1–6 ммоль/л | Без изменения (целевое значение) |
| Если любое единичное значение глюкозы плазмы: | |
| 3,1–4 ммоль/л (56–72 мг/дл) | -2 |
| <3,1 ммоль/л (<56 мг/дл) | -4 |
Если препарат Левемир® Пенфилл® используется как часть базис-болюсного режима, его следует назначать 1 или 2 раза в день, исходя из потребности пациента. Доза препарата Левемир® Пенфилл® определяется индивидуально в каждом конкретном случае.
Пациенты, которым требуется применение препарата дважды в день для оптимального контроля уровня гликемии, могут вводить вечернюю дозу либо во время ужина, либо перед сном. Коррекция дозы может быть необходима при усилении физической активности пациента, изменении его обычной диеты или при сопутствующем заболевании.
Лекарственный препарат Левемир® Пенфилл® может применяться как в виде монотерапии, так и в комбинации с болюсным инсулином. Его также можно применять в комбинации с пероральными гипогликемическими препаратами, а также дополнительно к существующей терапии лираглутидом.
В комбинации с пероральными гипогликемическими препаратами или в добавление к лираглутиду рекомендуется применять Левемир® Пенфилл® 1 раз в день, начиная с дозы 10 ЕД или 0,1–0,2 ЕД/кг. Лекарственный препарат Левемир® Пенфилл® можно вводить в любое удобное для пациента время в течение суток, однако определив время ежедневной инъекции, следует придерживаться установленного режима инъекций.
Левемир® Пенфилл® предназначен только для п/к введения. Левемир® Пенфилл® не следует вводить в/в, т.к. это может привести к тяжелой гипогликемии. Также следует избегать в/м введения препарата. Левемир® Пенфилл® не предназначен для использования в инсулиновых насосах.
Левемир® Пенфилл® вводится п/к в область бедра, передней брюшной стенки, плеча, дельтовидную или ягодичную область. Места инъекций следует регулярно менять даже при введении в одну и ту же область для уменьшения риска развития липодистрофии. Как и при использовании других препаратов инсулина, длительность действия зависит от дозы, места введения, интенсивности кровотока, температуры и уровня физической активности.
Особые группы пациентов
Как и при применении других препаратов инсулина, у пожилых пациентов и пациентов с почечной или печеночной недостаточностью следует более тщательно контролировать концентрацию глюкозы в крови и корректировать дозу инсулина детемир индивидуально.
Дети и подростки. Эффективность и безопасность применения Левемир® Пенфилл® у подростков и детей старше 2 лет подтверждена в ходе клинических исследований длительностью до 12 мес.
Перевод с других препаратов инсулина. Перевод с препаратов инсулина средней продолжительности действия и пролонгированных препаратов инсулина на препарат Левемир® Пенфилл® может потребовать коррекцию дозы и времени введения.
Как и при применении других препаратов инсулина, рекомендуется тщательный контроль концентрации глюкозы в крови во время перевода и в первые недели назначения нового препарата.
Возможно потребуется коррекция сопутствующей гипогликемической терапии (доза и время введения короткодействующих препаратов инсулина или доза пероральных гипогликемических препаратов).
Передозировка
Определенной дозы, обусловливающей передозировку инсулина, не установлено, однако гипогликемия может развиваться постепенно, если была введена слишком высокая доза для конкретного пациента.
Лечение: легкую гипогликемию пациент может устранить сам, приняв внутрь глюкозу, сахар или богатые углеводами продукты питания. Поэтому больным сахарным диабетом рекомендуется постоянно носить с собой сахар, сладости, печенье или сладкий фруктовый сок.
В случае тяжелой гипогликемии, когда пациент находится без сознания, следует ввести от 0,5 до 1 мг глюкагона в/м или п/к (может вводить обученный человек) либо в/в раствор декстрозы (глюкозы) (может вводить только медицинский работник). Также необходимо в/в вводить декстрозу в случае, если через 10–15 мин после введения глюкагона пациент не приходит в сознание. После восстановления сознания пациенту рекомендуется принять пищу, богатую углеводами, для профилактики рецидива гипогликемии.
Особые указания
Левемир® Пенфилл® является растворимым базальным аналогом инсулина, обладающим пролонгированным действием (до 24 ч).
В отличие от других препаратов инсулина, базис-болюсная терапия препаратом Левемир® Пенфилл® не приводит к увеличению массы тела.
Лечение лекарственным препаратом Левемир® Пенфилл® обеспечивает меньшее увеличение массы тела по сравнению с применением изофан-инсулина и инсулина гларгин.
Меньший по сравнению с изофан-инсулином риск ночной гипогликемии позволяет более интенсивно проводить титрацию дозы с целью достижения целевого показателя глюкозы крови в базис-болюсной терапии.
По сравнению с другими инсулинами, в частности изофан-инсулином, меньший риск наступления эпизодов легкой ночной гипогликемии позволяет более интенсивно проводить подбор дозы с целью достижения целевого показателя глюкозы крови при проведении лечения препаратом Левемир® Пенфилл® в комбинации с пероральными гипогликемическими препаратами.
Левемир® Пенфилл® обеспечивает лучший гликемический контроль (на основании измерения концентрации глюкозы плазмы натощак) по сравнению с применением изофан-инсулина.
Перед длительной поездкой, связанной со сменой часовых поясов, пациент должен проконсультироваться со своим лечащим врачом, поскольку смена часового пояса означает, что пациент должен принимать пищу и вводить инсулин в другое время.
Недостаточная доза препарата или прекращение лечения, особенно при сахарном диабете типа 1, может приводить к развитию гипергликемии или диабетического кетоацидоза. Как правило, первые симптомы гипергликемии появляются постепенно, в течение нескольких часов или дней. К этим симптомам относятся жажда, учащенное мочеотделение, тошнота, рвота, сонливость, покраснение и сухость кожи, сухость во рту, потеря аппетита, запах ацетона в выдыхаемом воздухе. При сахарном диабете типа 1 без соответствующего лечения гипергликемия приводит к развитию диабетического кетоацидоза и может привести к смерти.
Гипогликемия может развиться, если доза инсулина слишком высока по отношению к потребности в инсулине, при пропуске приема пищи или незапланированной интенсивной физической нагрузке.
После компенсации углеводного обмена, например при интенсифицированной инсулинотерапии, у пациентов могут измениться типичные для них симптомы-предвестники гипогликемии, о чем больные должны быть проинформированы. Обычные симптомы-предвестники могут исчезать при длительном течении сахарного диабета.
Сопутствующие заболевания, особенно инфекционные и сопровождающиеся лихорадкой, обычно повышают потребность организма в инсулине.
Коррекция дозы препарата может также потребоваться при наличии у пациента сопутствующих заболеваний почек, печени или нарушениях функции надпочечников, гипофиза или щитовидной железы.
Перевод больного с других препаратов инсулина. Перевод больного на новый тип или препарат инсулина другого производителя должен происходить под строгим врачебным контролем. При изменении концентрации, производителя, типа, вида (человеческий, аналог человеческого инсулина) и/или метода его производства может потребоваться коррекция дозы. Пациенты, переходящие на лечение препаратом Левемир® Пенфилл® с другого типа инсулина, могут нуждаться в изменении дозы по сравнению с дозами ранее применявшихся препаратов инсулина. Коррекция дозы может быть осуществлена при введении первой дозы или в течение первых нескольких недель или месяцев.
Реакции в местах введения. Как и при лечении другими препаратами инсулина, могут развиваться реакции в местах введения, что проявляется болью, покраснением, крапивницей, воспалением, гематомами, припухлостью и зудом. Регулярная смена места инъекции в одной и той же анатомической области может уменьшить симптомы либо предотвратить развитие реакции. Реакции обычно исчезают в течение от нескольких дней до нескольких недель. В редких случаях реакции в местах введения требуют прекращения лечения.
Одновременное применение препаратов группы тиазолидиндиона и препаратов инсулина. Сообщалось о случаях развития хронической сердечной недостаточности при лечении пациентов тиазолидиндионами в комбинации с препаратами инсулина, особенно при наличии у таких пациентов факторов риска развития хронической сердечной недостаточности. Следует учитывать данный факт при назначении пациентам комбинированной терапии тиазолидиндионами и препаратами инсулина. При назначении такой комбинированной терапии необходимо проводить медицинские обследования пациентов на предмет выявления у них признаков и симптомов хронической сердечной недостаточности, увеличения массы тела и наличия отеков. В случае ухудшения у пациентов симптоматики сердечной недостаточности лечение тиазолидиндионами необходимо прекратить.
Влияние на способность к управлению автомобилем и работе с механизмами. Способность пациентов к концентрации внимания и скорость реакции могут нарушаться из-за гипогликемии, что может представлять опасность в тех ситуациях, когда эти способности особенно необходимы (например при управлении автомобилем или работе с машинами и механизмами). Пациентам необходимо рекомендовать предпринимать меры для предупреждения развития гипогликемии при вождении автомобиля и работе с механизмами. Это особенно важно для пациентов с отсутствием или снижением выраженности симптомов-предвестников развивающейся гипогликемии или страдающих частыми эпизодами гипогликемии. В этих случаях следует рассмотреть целесообразность управления автомобилем или выполнения подобных работ.
Форма выпуска
Раствор для подкожного введения, 100 ЕД/мл. В картриджах из стекла 1 гидролитического класса, укупоренных дисками из бромбутиловой резины с одной стороны и поршнями из бромбутиловой резины с другой, по 3 мл; в блистерах из ПВХ/фольги алюминиевой по 5 картриджей; в пачке картонной 1 блистер.
Производитель
Ново Нордиск А/С.
Ново Алле, DK-2880, Багсваерд, Дания.
Представительство Ново Нордиск А/С.
119330, Москва, Ломоносовский пр-т, 38, оф. 11.
Тел.: (495) 956-11-32; факс: (495) 956-50-13.
Условия отпуска из аптек
По рецепту.
Условия хранения препарата Левемир® Пенфилл®
Хранить в недоступном для детей месте.